Det har länge varit känt att alla molekyler har två lika och motsatta laddningar som är separerade med ett visst avstånd. I fallet med sådana polära molekyler sammanfaller inte centrum för negativ laddning med centrum för positiv laddning. Polaritetsgraden i sådana kovalenta molekyler kan beskrivas med termen Dipole Moment, som i huvudsak är måttet på polaritet i en polär kovalent bindning.
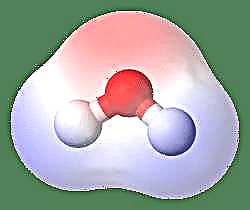
Det enklaste exemplet på en dipol är en vattenmolekyl. En vattenmolekyl är polär på grund av ojämn delning av dess elektroner i en "böjd" struktur. Vattenmolekylen bildar en vinkel med väteatomer vid spetsarna och syre i topppunkten. Eftersom syre har en högre elektronegativitet än väte, har molekylens sida med syreatomen en partiell negativ laddning medan väte i mitten har en delvis positiv laddning. På grund av detta pekar riktningen på dipolmomentet mot syre.
På fysikens språk är det elektriska dipolmomentet ett mått på separationen av positiva och negativa elektriska laddningar i ett laddningssystem, det vill säga ett mått på laddningssystemets totala polaritet - dvs separationen av molekylernas elektriska laddning, som leder till en dipol. Matematiskt, och i det enkla fallet med tvåpunktsladdningar, en med laddning + q och en med laddning? Q, kan det elektriska dipolmomentet p uttryckas som: p = qd, där d är förskjutningsvektorn som pekar från negativ laddning till den positiva avgiften. Således pekar den elektriska dipolmomentvektorn p från den negativa laddningen till den positiva laddningen.
Ett annat sätt att titta på det är att representera Dipole Moment med den grekiska bokstaven m, m = ed, där e är den elektriska laddningen och d är separationsavståndet. Det uttrycks i enheterna i Debye och skrivs som D (där 1 Debye = 1 x 10-18e.s.u cm). Ett dipolmoment är en vektorkvantitet och representeras därför av en liten pil med en svans vid det positiva mitten och huvudet som pekar mot ett negativt centrum. När det gäller en vattenmolekyl är Dipolmomentet 1,85 D, medan en molekyl saltsyra är 1,03 D och kan representeras som:
Vi har skrivit många artiklar om dipolögonblick för Space Magazine. Här är en artikel om vad vatten är gjord av, och här är en artikel om molekyler.
Om du vill ha mer information om dipolmoment kan du kolla in de här artiklarna från Hyperphysics and Science Daily.
Vi har också spelat in ett helt avsnitt av Astronomy Cast som handlar om molekyler i rymden. Lyssna här, avsnitt 116: Molecules in Space.
källor:
http://en.wikipedia.org/wiki/Electric_dipole_moment
http://en.wikipedia.org/wiki/Dipole
http://www.tutorvista.com/content/chemistry/chemistry-iii/chemical-bonding/degree-polarity.php
http://hyperphysics.phy-astr.gsu.edu/hbase/electric/dipole.html#c1
http://en.wikipedia.org/wiki/Water_molecule